El 18 de octubre pasado, mediante la Resolución N° 085-024/12, el Consejo de Administración del IPS autoriza el llamado a licitación N° 110/12 “Adquisición de medicamentos varios para el IPS - segundo grupo”. En la lista se encuentra ranitidina en sus dos presentaciones, que son 150 mg en comprimidos y 150 mg inyectables.
Sin embargo, recién trece días después, el 30 de octubre, mediante la Resolución N° 088-036/12, el Consejo aprobó las modificaciones al vademécum institucional de medicamentos.
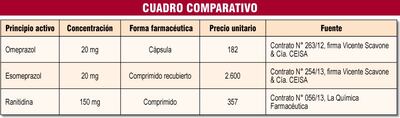
En este documento se aprueba la inclusión de la ranitidina y el esomeprazol. Además, se excluye al omeprazol. Estas drogas son utilizadas como un protector del estómago y para tratar problemas gástricos.
El Consejo estaba integrado por José Disnardo Zarza, Dr. José Bellassai, Ing. Hugo Cataldo, Dr. Remberto Cáceres y Jorge Alvarenga.
Estas personas aprobaron la modificación sin la aprobación de la Asesoría Médica, que en ese entonces estaba a cargo del Dr. Antonio Barrios, actual ministro de Salud.
Este les recordó, memorando mediante, que se realizó el llamado a la compra de ranitidina sin aprobación. Además la Asesoría Médica recomendó excluir del cuadro básico de medicamentos tanto los comprimidos como los inyectables por ser fármacos de poco efecto en la actualidad.
Además, dejó constancia de que la exclusión del omeprazol se realizó sin la anuencia del jefe de Servicio de Gastroenterología, Dr. Néstor Gill Petta. Tampoco dio su aprobación para la inclusión del esomeprazol.
Esta serie de irregularidades serán denunciadas ante la fiscalía la próxima semana, adelantó el director de Auditoría, Fernando Flecha.