12 de marzo de 2026
Dirección Nacional de Vigilancia Sanitaria (Dinavisa)

Dinavisa incauta miles de envases para clonar remedios en Aeropuerto Silvio Pettirossi
En un operativo contra la falsificación de fármacos, Dinavisa e investigadores del Ministerio Público incautaron 80.000 frascos viales para insumos médicos y maquinaria de sellado en el Aeropuerto Silvio Pettirossi. El hallazgo se produce tras la alerta sanitaria por lotes falsos de un inyectable para adelgazar.

Dinavisa suspende a conocido supermercado del centro de Asunción
La Dirección Nacional de Vigilancia Sanitaria (Dinavisa) realizó una inspección a un conocido supermercado del centro de Asunción y tras verificar denuncias realizadas por los consumidores, ordenó la suspensión y prohibición de comercialización de algunos productos.
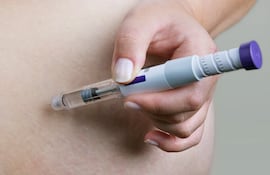
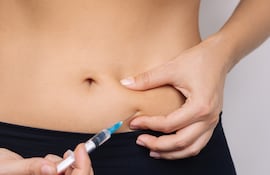
Dinavisa alerta sobre “riesgo grave” del uso de adelgazante sin receta ni control
El director de Vigilancia de Medicamentos de Dinavisa, Óscar Allende, advirtió que los fármacos utilizados para tratar obesidad y diabetes deben venderse únicamente bajo receta médica y dentro de una cadena legal que garantice su conservación. Alertó además sobre la circulación de productos falsificados, mal conservados o comercializados por vías ilegales, que pueden representar un grave riesgo para la salud.

Empresa retira del mercado lote de productos destinados a bebés
La Dirección Nacional de Vigilancia Sanitaria Paraguay informó que la empresa Nestlé Paraguay S.A. comenzó a retirar la Fórmula Infantil NAN Optipro 1 con HMO, en sus presentaciones lata de 400 gramos y lata de 800 gramos. Esto, debido a la posible presencia de una toxina producida por el microorganismo Bacillus cereus.